A limitação ao direito de uso de marca registrada como nome de medicamento - a resolução ANVISA RDC nº 351/2005
Por meio da Resolução da Diretoria Colegiada nº 351, de 28.12.2005 ("RDC 351/2005"), publicada no Diário Oficial da União em 2.1.2006, a Agência Nacional de Vigilância Sanitária - ANVISA determinou que diversos laboratórios farmacêuticos procedam, no prazo de 90 (noventa) dias, à modificação dos nomes de mais de 900 (novecentos) medicamentos comercializados no Brasil, sob pena de cancelamento dos registros desses produtos e caracterização de infração sanitária.
quarta-feira, 8 de março de 2006
Atualizado em 7 de março de 2006 15:48
A limitação ao direito de uso de marca registrada como nome de medicamento - a resolução ANVISA RDC nº 351/2005
André Zonaro Giacchetta*
Ciro Torres Freitas*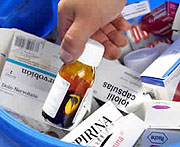 1. - Por meio da Resolução da Diretoria Colegiada nº 351, de 28.12.2005 ("RDC 351/2005"), publicada no Diário Oficial da União em 2.1.2006, a Agência Nacional de Vigilância Sanitária - ANVISA determinou que diversos laboratórios farmacêuticos procedam, no prazo de 90 (noventa) dias, à modificação dos nomes de mais de 900 (novecentos) medicamentos comercializados no Brasil, sob pena de cancelamento dos registros desses produtos e caracterização de infração sanitária.
1. - Por meio da Resolução da Diretoria Colegiada nº 351, de 28.12.2005 ("RDC 351/2005"), publicada no Diário Oficial da União em 2.1.2006, a Agência Nacional de Vigilância Sanitária - ANVISA determinou que diversos laboratórios farmacêuticos procedam, no prazo de 90 (noventa) dias, à modificação dos nomes de mais de 900 (novecentos) medicamentos comercializados no Brasil, sob pena de cancelamento dos registros desses produtos e caracterização de infração sanitária.
2. - Essa determinação resultou de um "julgamento de marcas preferenciais"1 levado a termo pela própria ANVISA, sob o pretexto de solucionar supostos conflitos entre nomes considerados semelhantes atribuídos a diferentes medicamentos. Para tanto, em 27.4.2005, a ANVISA fez publicar no Diário Oficial da União um Edital de Notificação indicando diversos medicamentos, devidamente registrados na ANVISA, cujos nomes foram considerados conflitantes, de acordo com as regras estabelecidas no item 3 da RDC 333/2003, editada pela ANVISA em 19.11.2003.2
3. - De acordo com o Edital de Notificação, os laboratórios farmacêuticos deveriam apresentar à ANVISA documentação referente à propriedade das marcas usadas para identificar os medicamentos listados, devendo constar a data de concessão de eventual registro de marca pelo Instituto Nacional da Propriedade Industrial - INPI ou, não sendo o nome do medicamento objeto de registro de marca concedido pelo INPI, a data de registro do produto na ANVISA.
4. - O Edital de Notificação da ANVISA indicou também os "critérios para julgamento da marca preferencial", dispondo que seriam consideradas detentoras das marcas, frente àquelas consideradas semelhantes, as empresas que: (i) detivessem registro de marca mais antigo no INPI; (ii) na ausência deste, as que tivessem registrado "o nome de marca"3 na ANVISA com maior anterioridade; ou (iii) no caso de "transferência de marca ou nome comercial", as que apresentassem prova de cancelamento do registro anterior, de acordo com a legislação vigente.
5. - Por fim, o Edital de Notificação estabeleceu que após a divulgação do resultado do julgamento no site da ANVISA, os laboratórios farmacêuticos que não obtivessem o status de "preferencial" deveriam providenciar a modificação do(s) nome(s) do(s) medicamento(s), apresentando, inclusive, os textos de bula, rótulo e/ou cartucho adequados à nova denominação. A divulgação do resultado do julgamento realizado pela ANVISA ocorreu, de fato, por meio da RDC 351/2005.
6. - Embora indique como fundamento dispositivos da Lei nº 6.360, de 23.9.1976, e do Decreto nº 79.094, de 5.1.1977, que vedam a adoção de nomes iguais ou semelhantes para diferentes medicamentos, a determinação imposta pela ANVISA por meio da RDC 351/2005, além de não observar princípios inerentes à atividade administrativa, implica, particularmente em relação aos medicamentos cujos nomes são objeto de registros de marca concedidos pelo INPI, ofensa a direitos de propriedade industrial dos laboratórios farmacêuticos.
7. - O registro de marca concedido pelo INPI é atributivo de propriedade e assegura ao titular o direito ao uso exclusivo da marca, em todo o território nacional4. Ainda que a Lei nº 6.360/76 e o Decreto nº 79.094/77 atribuam competência à ANVISA para obstar o registro de medicamentos com denominações passíveis de causar erro, a determinação de mudança de nome protegido por registro de marca, editada pela ANVISA em desacordo com a legislação, caracteriza restrição indevida dos direitos dos titulares das marcas registradas perante o INPI.
8. - A RDC 351/2005 aponta os medicamentos cujos nomes a ANVISA entende devam ser alterados, mas não explicita de forma individualizada as razões para tal determinação. Na prática, a empresa fabricante de um medicamento incluído na RDC 351/2005 sequer é cientificada a respeito de qual medicamento teve o nome julgado "preferencial" em relação ao seu produto, tampouco dos elementos específicos usados como fundamento para o "julgamento" da ANVISA, tais como a existência e as particularidades de eventual registro de marca concedido pelo INPI.
9. - A não indicação dos fundamentos que levaram a ANVISA a determinar a alteração do nome de determinado medicamento impossibilita o próprio cumprimento da RDC 351/2005, posto que o respectivo fabricante, não tendo conhecimento do(s) nome(s) supostamente colidente(s) com o do seu produto, poderá incidir em nova colidência ao requerer o registro de um novo nome, não cumprindo a Resolução da ANVISA.
10. - Além da ausência de suficiente exposição dos fundamentos de fato para a determinação de mudança do nome de cada um dos medicamentos que indica, a RDC 351/2005 restringe direitos dos fabricantes dos medicamentos sem que lhes tenha sido assegurada qualquer oportunidade de defesa. Em outras palavras, a ANVISA impôs a alteração de nomes de medicamentos previamente registrados e regularmente comercializados, sob pena de cancelamento de registro dos produtos e caracterização de infração sanitária, independentemente de qualquer processo administrativo que assegurasse aos fabricantes a ampla defesa e o contraditório.
11. - Há que se ressaltar também que os medicamentos indicados na RDC 351/2005 foram registrados pela ANVISA sem que esta tenha obstado a adoção dos respectivos nomes, como determinam a Lei nº 6.360/76 e o Decreto nº 79.094/77 na hipótese de constatação de denominações semelhantes ou passíveis de causar erro. A ordem de mudança dos nomes desses medicamentos, por meio da RDC 351/2005, denota uma tentativa da ANVISA de sanar a própria omissão, como se os registros tivessem ocorrido em desacordo com a legislação, revestindo-se, pois, de nulidade.
12. - Assim, ao determinar a alteração de nomes de medicamentos regularmente registrados pela própria ANVISA, comercializados há longa data - inclusive nomes protegidos por registros de marca concedidos pelo INPI - a RDC 351/2005 afeta outro elemento característico da atividade administrativa, qual seja, a estabilidade das situações jurídicas, afrontando o princípio da segurança jurídica por tentar reverter e tornar sem efeito ato a que a própria Administração Pública atribuiu legitimidade por prolongado lapso temporal, perante toda a coletividade.
13. - A motivação, a ampla defesa, o contraditório e a segurança jurídica são princípios abrigados na Constituição Federal e cuja obediência se impõe à Administração Pública por disposição expressa da Lei nº 9.784, de 29.1.1999. A ordem de mudança dos nomes de medicamentos registrados na ANVISA, por meio da RDC 351/2005, especialmente em relação àqueles cuja denominação é protegida por registro de marca concedido pelo INPI, fere os princípios mencionados e viola dispositivos legais de aplicação obrigatória à Administração Pública.
14. - Conseqüência disso é a restrição indevida dos direitos assegurados aos laboratórios farmacêuticos pelos registros de marca concedidos pelo INPI, tendo por objeto os nomes de seus medicamentos. A RDC 351/2005, ferindo princípios e dispositivos legais obrigatórios para a Administração Pública, não apenas impede e limita o exercício do direito ao uso exclusivo de marca registrada que é assegurado aos titulares, como veda esse uso, tornando sem efeito o registro de marca expedido em conformidade com a legislação vigente pelo órgão competente - o INPI.
____________
1 A legislação brasileira não prevê a existência de "marcas preferenciais" - termo desprovido de conotação técnica.
2 RDC 333/2003 - "3. Nome Comercial: A formação de nomes comerciais para medicamentos deve seguir os critérios abaixo: 3.1. - O nome não pode ser assemelhado ou gerar confusão com outro nome de medicamento já registrado ou protocolado na ANVISA na forma impressa, manuscrita ou falada. 3.2. - O nome comercial não pode causar confusão ou semelhança com a denominação genérica da substância ativa conforme DCB, DCI, CAS ou sinonímias destes adotadas para estes compostos. 3.3. - O nome comercial não pode causar confusão ou semelhança com quaisquer letras ou números na forma impressa, manuscrita ou falada. 3.4. - Pode ser utilizado nome assemelhado a outro já registrado desde que se diferencie por no mínimo 3 letras distintas, presentes ou ausentes, limitando a probabilidade de haver confusão na escrita para resguardar a identidade do produto realmente prescrito. (.)"
3 O termo "nome de marca" é usado pela ANVISA para fazer referência a nome de medicamento.
4 Lei 9.279/96 - "Art. 129 - A propriedade da marca adquire-se pelo registro validamente expedido, conforme as disposições desta Lei, sendo assegurado ao titular seu uso exclusivo em todo o território nacional, observado quanto às marcas coletivas e de certificação o disposto nos arts. 147 e 148."
_________________
*Advogados do escritório Pinheiro Neto Advogados
* Este artigo foi redigido meramente para fins de informação e debate, não devendo ser considerado uma opinião legal para qualquer operação ou negócio específico.
© 2006. Direitos Autorais reservados a PINHEIRO NETO ADVOGADOS



